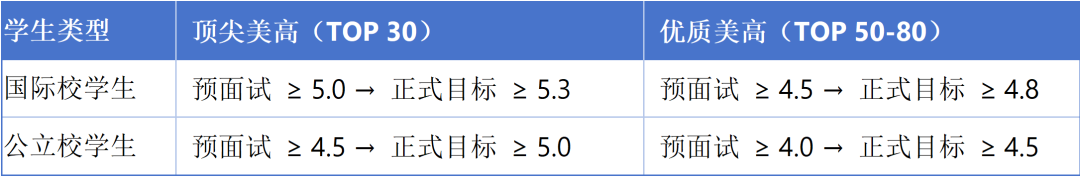
01、招生要求

澳门大学健康科学学院已公布2026/2027学年生物医药哲学博士项目的具体条件。学历方面,申请人需具备相关领域硕士学位;本科学历者若毕业于双一流高校或一流学科专业且GPA达3.0以上(4.0制),亦具备申请资格。语言能力需满足以下任一标准:托福网考不低于80分,雅思总分6.0且各单项5.5以上,或大学英语六级430分以上。值得注意的是,语言成绩自考试日期起两年内有效。
申请流程分两步:申请人须先行浏览学院官网导师名录,选定指导教授并建立联系;其后在指定报名时段内通过澳门大学网上申请系统完成注册。材料初审通过者将获面试通知,最终录取结果综合学术背景、研究潜力及面试表现而定。项目学制四年,首年集中完成必修课程,次年通过资格考试方可正式开展论文研究。
02、研究方向
Hanming Shen教授担任健康科学学院副院长与讲座教授,其实验室长期专注于肿瘤生物学核心机制探索,近年来取得突破性进展。
首先,自噬与溶酶体调控网络。团队揭示ATG16L1蛋白去乙酰化是启动LC3相关溶酶体微自噬的 prerequisite事件(Autophagy, 2025)。同期Nature Structural & Molecular Biology论文阐明CtBP-TRIM28转录抑制复合物通过阻断自噬体形成,在表观遗传层面驱动肿瘤转移。这提示自噬调控存在多层交叉对话。
其次,线粒体自噬的机制创新。PNPLA7被确认为Parkin线粒体招募的新型介导因子,该发现发表于Nature Communications(2025),扩展了PINK1-Parkin通路的调控维度。另一项Autophagy(2025)研究构建SMAD3-PINK1正向反馈回路模型,揭示TGF-β信号与线粒体质量控制之间的偶联关系。
第三,代谢重编程的可塑性研究。葡萄糖代谢通过O-GlcNAc修饰直接调控PINK1活性,实现代谢通量与线粒体自噬的即时联动(International Journal of Biological Sciences, 2025)。更具转化价值的是,整合热蛋白质组与热邻近共聚集分析(TPP-TPCA)技术,首次鉴定ATP6V1C1亚基为veratramine的天然靶点,为V-ATPase抑制剂的开发提供结构基础。
03、有想法
基于Shen教授研究体系,未来博士生可纵深挖掘以下方向:
方向一:PNPLA7-Parkin轴的代谢-免疫交叉调控
Nature Communications(2025)数据显示PNPLA7在脂肪组织中介导线粒体自噬并抑制棕色化。延伸思考:肿瘤微环境中的癌相关脂肪细胞是否共享该机制?低氧微环境可能通过HIF-1α转录抑制PNPLA7,导致损伤线粒体清除障碍,累积的mtDNA进而激活cGAS-STING先天免疫通路。该设想将代谢适配与免疫监视串联,可验证PNPLA7作为代谢-免疫检查点的可行性。
方向二:MDVs代谢物分拣的决策逻辑
Life Metabolism(2025)提出线粒体衍生囊泡(MDVs)桥接代谢信号与线粒体适应度。关键科学问题:代谢物浓度梯度是否构成MDVs的"分拣密码"?可验证α-酮戊二酸/琥珀酸比值是否通过特定受体蛋白(如SNX9或TOM20变异体)调控MDVs货物选择性。此机制若获证实,可推广至内质网、过氧化物酶体等细胞器的质量控制体系,建立普适性的代谢-细胞器通讯模型。
方向三:ATP6V1C1抑制的时空精准化
IJBS(2025)证实veratramine破坏V-ATPase功能。深化方向在于:不同肿瘤对溶酶体酸化的依赖程度存在异质性。可设计肿瘤微酸响应的纳米递送系统,实现ATP6V1C1抑制剂的组织特异性释放。同步开发pH比率型荧光探针,绘制单细胞分辨率的溶酶体pH图谱,量化V-ATPase抑制后自噬流阻滞的时空动态,为精准干预提供可视化依据。
方向四:自噬-代谢网络在转移前微环境的远程调控
整合NSMB(2025)与Autophagy(2025)成果,CtBP-TRIM28轴与ATG16L1去乙酰化构成自噬调控的两极。假设原发灶分泌的外泌体携带特定miRNA(如miR-199a-3p),远程抑制肺部成纤维细胞自噬活性,协同改造转移靶器官的代谢基质。通过代谢流分析与谱系追踪技术,可揭示循环肿瘤细胞定植的代谢生态位构建机制,为阻断转移提供早期干预靶点。